Por Silvia Reis
A documentação em geral é uma parte essencial de um sistema de gestão da qualidade (SGQ). E estes documentos devem ter controles seguros, confiáveis e, se necessário, validados, de forma a garantir a integridade do registro durante todo o período de retenção garantindo assim a qualidade final de um produto ou processo.
E estes documentos, que podem ser eletrônicos, manuais ou mistos (parte manual parte eletrônica), incluem:
- Procedimentos implementados, Comunicados etc.;
- Registros em geral;
- Cálculos e Dados brutos;
- Calibrações, Verificações, Validações e Qualificações;
- Observações originais; v Resultados e Relatórios manuais ou de equipamentos;
- Especificações, Testes, Fórmulas etc.;
- Listas Mestras.
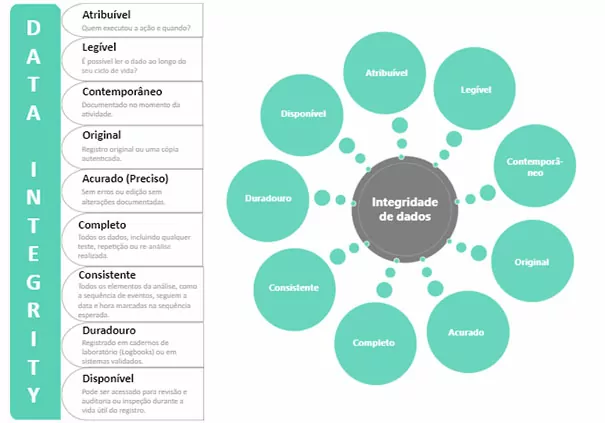
E o princípio que rege esta parte do SGQ foi estabelecido e identificado pelo FDA (Food and Drug Administration) como ALCOA. Segundo esse princípio, um dado deve possuir as seguintes características:
Atribuível: o dado gerado ou coletado deve estar atribuído a quem realizou a ação e quando a ação foi realizada. Exemplos:
– Sistema eletrônico: deve-se ter logins e senhas individuais, identificando facilmente quem inseriu, quem alterou ou quem excluiu um determinado dado em uma trilha de auditoria (também chamada de audit trail).
– Sistema manual: os registros devem conter assinaturas ou rubricas datadas, e todas elas devem ser únicas e registradas em um documento, que pode ser um logbook, atribuindo a assinatura e rubrica a apenas uma pessoa.
Legível: o dado coletado deve ser registrado de forma legível e permanente. Exemplos:
– Sistema eletrônico: os registros devem ser verificados periodicamente quanto à legibilidade[VB1] (O documento em meio eletrônico precisar estar em formato que possa ser aberto e lido por outras pessoas, como o PDF.), as trilhas de auditoria devem ser facilmente inteligíveis e impossíveis de serem modificadas por um usuário.
– Sistema manual: os registros devem ser feitos de forma indelével, que não se apaguem(são proibidos registros com lápis ou canetas que apaguem e uso de corretivos). Além disso, erros ou rasuras devem ser corrigidos apenas com um traço, justificados, assinados e datados.
Contemporâneo: o dado deve ser registrado quando a ação ocorre. Exemplos:
– Sistema eletrônico: o sistema deve gerar automaticamente o registro de data e hora da entrada dos dados, bem como nas assinaturas eletrônicas. Mudanças de horários nos relógios dos sistemas não podem ser permitidas. É proibido salvar ou encaminhar dados de registros.
– Sistema manual: os registros devem ser realizados no momento da atividade, não sendo permitidos registros retroativos. É proibido gerar fotocópias de registros sem autorização.
Original: o dado deve ser anotado diretamente no sistema, no logbook ou folha de registro, evitando anotações provisórias e posterior transcrição desses dados. Exemplos:
– Sistema eletrônico: os metadados devem ser revisados periodicamente e o sistema deve impedir a exclusão de dados originais.
– Sistema manual: não devem ser permitidos o uso de rascunho ou notas adesivas na área de BPx. Os documentos originais devem ser armazenados de forma controlada e segura, e devem estar disponíveis prontamente para uma inspeção.
Acurado: o dado gerado deve estar livre de erros, completo e verdadeiro, refletindo exatamente as ações determinadas no processo. Exemplos:
– Sistema eletrônico: os sistemas devem ser validados e revisados periodicamente. Os dados do sistema devem ser protegidos contra alterações não autorizadas.
– Sistema manual: os desvios e resultados fora da especificação devem ser investigados. Os instrumentos devem sempre estar calibrados. Recomenda-se verificações secundárias a fim de verificar a precisão dos dados críticos.
Além deste conceito, existe também o ALCOA+, criado pela PIC/S (Pharmaceutical Inspection Co-operation Scheme), onde o “+” traz mais 4 quesitos para a qualificação de um dado:
Completo: o dado deve estar completo, ou seja, mesmo testes invalidados devem constar no relatório final.
Consistente: o dado registrado não pode ser modificado ao longo do ciclo de vida.
Duradouro: o dado não pode se perder com o tempo, por exemplo dados impressos em impressoras térmicas.
Disponível: o dado deve sempre estar disponível durante todo o seu ciclo de vida, por exemplo em uma mudança de sistema não se pode perder dados.
E para uma melhor visualização no dia-a-dia, seguem alguns exemplos de falhas na integridade de dados: Ignorar ou omitir determinados dados de um conjunto de dados;
- Falsificação intencional de dados (ocultar, substituir dados originais, reescrever registros etc.);
- Testes não oficiais;
- Exclusão de dados com falhas;
- Falsificação de dados para liberação de lotes;
- Gravação de amostras ou pesos em papel de rascunho;
- Resultados fora da especificação não investigados ou não relatados;
- Nenhuma restrição ou proteção de dados eletrônicos, acessos sem senhas individuais;
- Produto liberado e não registrado;
- Entradas pré ou pós datadas;
- Registros retroativos;
- Uso de pen drives.
E como podemos prevenir problemas com integridade de dados?
- Mantendo pessoal técnico competente e treinado;
- Treinamentos eficazes para novos colaboradores, com abordagem cultural da empresa, com correções de mentalidade e moldagem destes recém contratados de organizações com culturas diferentes;
- Uma educação continuada para uma boa adesão aos procedimentos e políticas em vigor;
- Conscientização e interpretação correta dos regulamentos e requisitos de BPF.
Em todas as fases de um processo ou ciclo de vida de um documento, que envolva dados (como: criar, gravar, checar, processar, revisar, analisar, reportar, transferir, armazenar, consultar ou monitorar), até que ele não seja mais útil e se torne obsoleto e finalmente excluído, a integridade de dados deve estar presente, esteja ele em formato eletrônico ou manual.
Além disso, deve-se planejar uma avaliação, monitoramento e gerenciamento destes dados e seus riscos levando em consideração sua criticidade. Ao conjunto dos temas acima citados, damos o nome de “governança de dados” e todos em uma organização são responsáveis, desde a Alta Diretoria, disponibilizando recursos e tomada de decisão, até o Analista que alimenta estes dados.
A integridade dos dados é crucial na implementação de um SGQ e uma vez ignorada esta importância, não será possível garantir um sistema robusto, com entrega de produtos ou serviços eficazes e de alta qualidade.